UJIAN
AKHIR SEMESTER
MATA
KULIAH : KIMIA BAHAN ALAM
SKS
: 2
DOSEN
: Dr. Syamsurizal, M.Si
WAKTU
: 22-29
Desember 2012
PETUNJUK :
Ujian ini open book. Tapi tidak diizinkan mencontek, bilamana ditemukan, maka
anda dinyatakan GAGAL. Jawaban anda diposting di bolg masing-masing.
1. Jelaskan dalam jalur biosintesis
triterpenoid, identifikasilah faktor-faktor penting yang sangat menentukan
dihasilkannya triterpenoid dalam kuantitas yang banyak.
Jawab:
Terpenoid
merupakan bentuk senyawa dengan struktur yang besar dalam produk alami yang
diturunkan dan unit isoprene (C5)yang bergandengan dalam model kepala ke ekor,
sedangkan unit isoprene diturunkan dari metabolism asam asetat oleh jalur asam
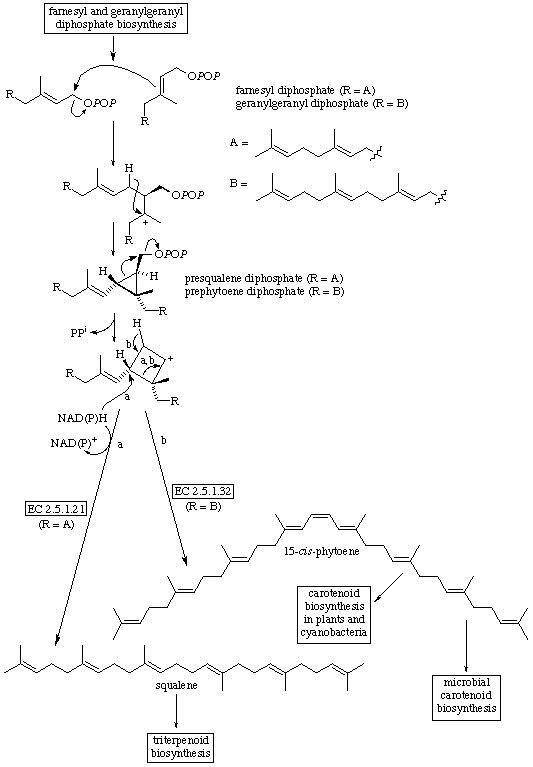
mevalonat (MVA). Jalur bosintasis triterpenoid dapat dililat dibawh ini
Jalur
biosentesis triterpenoid dimulai dari asetil koenzim A melakukan kodensasi jenis
aldol menghasilkan rantai karbon bercabang sebagai mana ditemukan pada asam
mevalinat, dan terjadi reaksi selanjutnya berupa reaksi fosforilasi, eliminasi
asam fosfat dan dekarboksilasi menghasilkan isopentenil piroposfat (IPP) yang
selanjutnya erisomerisasi menjadi dimetil alil pirofosfat (DMAPP) oleh enzim
isomerasi.
IPP
yang dimana merupakan unit isopern aktif bergabung dengan DMAPP antara kepala
dan ekor ini terjadi disebabkan oleh serangan elektron dari ikatan rangkap IPP
terhadap atom karbon dari DMAPP yang kekurangan elektron diikuti oleh
penyingkiran ion piro fosfat yang menghasilkan geranil. setelah itu maka
terbentuklah aqualane triterpenoid yang mana mengalami penataan struktur .
Secara umum biosintesis
terpenoid terjadinya melalui 3 reaksi dasar :
1. Pembentukan isopren aktif
berasal dari asam asetat melalui asam mevalonat
2. Penggabungan ekor dan
kepala 2 unit isopren akan membentuk mono-, seskui-, di-, dan
poli-terpenoid
3. Penggabungan ekor dan ekor dari unit C15 atau C20 menghasilkan triterpenoid dan steroid
3. Penggabungan ekor dan ekor dari unit C15 atau C20 menghasilkan triterpenoid dan steroid
Faktor
- faktor yang mempengaruhi banyak sedikitnya hasil dari triterpenoid dalam
jalur biosintasis triterpenoid adalah :
1.
Pada saat penggabungan kepala dan ekor dua unit isoprene, penggabungan
ekor dan ekor dari unit C-15 atau C-20 menghasilkan triterpenoid dan steroid,
pembentukan senyawa-senyawa monoterpen dan senyawa terpenoida yang berasal dari
penggabungan 3,3 dimetil allil pirofosfat dengan isopentenil pirofosfat.
2.
Enzim yang bekerja, pH dan temperatur menjadi faktor penting keberhasilan
terbentuknya senyawa hasil proses biosintesis seperti, senyawa triterpenoid.
2.
Jelaskan dalam penentuan struktur flavonoid, kekhasan signal dan intensitas
serapan dengan menggunakan spektrum IR dan NMR. Berikan dengan contoh
sekurang-kurangnya dua struktur yang berbeda?
Jawab:
Kekhasan
signal dan intensitas serapan struktur Flavonoid dengan menggunakan spektrum IR
dan NMR adalah berdasarkan spectrumnya yang terdiri atas 2 maksimal pada
rentang 240 - 280 nm (pita II) dan 300 - 550 nm (pita I) kedudukan yang tepat
dan kekuatan nisbi maksimal tersebut memberikan informasi yang berharga
mengenai sifat flavonoid dan pola oksigenasi. Ciri khas dalam spektrum tersebut
adalah memberikan puncak relatif rendah pada pita I untuk flavonoid golongan
hidroflavon dan isoflavon dan untuk antosianin dan khalkon memberikan puncak
yang relatif tinggi.
Spektrum
RMI – 1H terlihat terutama di daerah 0 – 10 ppm medan bawah dari sinyal acuan
tetrametilsilan (yang berdasarkan perjanjian ditetapkan pada 0 ppm). Hanya
proton yang menghasilkan sinyal (beresonansi) di daerah ini dan proton yang
secara kimia sama memberikan sinyal yang sama. Ukuran sinyal (integrasi)
berbanding lurus dengan jumlah proton yang menghasilkan sinyal. Pada
identifikasi flavanoid Spektroskopi Resonansi Magnet Inti (RMI – 1H ) digunakan
khas untuk :
·
Penentuan
pola oksigenasi (pada ketiga lingkar).
·
Penentuan jumlah gugus metoksi (dan kedudukannya).
·
Pembedaan isoflavon, flavonon, dan
dihidroflavonol.
·
Penentuan
jumlah gula yang ada (dan penentuan apakah ikatannya α – atau β ).
·
Pendeteksian rantai samping hidrokarbon
seperti –CH3 yang terikat pada C dan prenil yang terikat pada
C (atau O).
Seperti
pada gambar yang strukturnya di bawah ini :
Isoflavon
Flavon
3.
Dalam isolasi alkaloid, pada tahap awal dibutuhkan kondisi asam atau basa.
Jelaskan dasar penggunaan reagen tersebut, dan berikan contohnya
sekurang-kurangnya tiga macam alkaloid?
Jawab:
Pada
tahap awal isolasi alkaloid dibutuhkan kondisi asam karena dengan penambahan
asam organik maka ekstrak akan menghasilkan garam atau penambahan asam berguna
untuk mengikat alkaloid dengan garam nya. Penambahan basa berguna untuk
membebaskan ikatan garam menjadi alkaloida yang bebas.
Contohnya
adalah sebagai berikut ini :
Ø Isolasi alkaloid dilakukan dengan
metode ekstraksi. Bahan tanaman, terutama biji dan daun sering banyak
mengandung lemak, lilin yang sangat nonpolar. Karena, senyawa-senyawa tersebut
dipisahkan dari bahan tanaman sebagai langkah awal dengan cara pelarutan dengan
petrolium eter. Kebanyakan alkaloid tidak larut dalam petrolium eter. Namun,
ekstrak harus selalu dicek untuk mengetahui adanya alkaloid dengan menggunakan
salah satu pereaksi pengendap alkaloid. Bila sejumlah alkaloid larut dalam
pelarut petrolium eter, maka bahan tanaman pada awal ditambahkan dengan asam
untuk mengikat alkaloid sebagai garam nya. Prosedurini telah digunakan untuk
mengekstrak ergotamin dari cendawan ergot.
Ø prinsip pengerjaan dengan azas
keller yaitu alkaloida yang terdapat dalam suatu bakal sebagai bentuk garam,
dibebaskan dari ikatan garam tersebut menjadi alkaloida yang bebas. Untuk itu
ditambahkan basa lain yang lebih kuat dari pada alkaloida tadi. Basa yang
dipakai tidak boleh terlalu kuat karena alkaloid pada umumnya kurang stabi.
Pada pH tnggi ada kemungkinan akan terurai, terutama dalam keadaan bebas. Bahan
tumbuhan dapat dibebaskan dengan natrium karbonat.
Ø Nikotina dapat dimurnikan dengan
cara penyulingan uap dari larutan yang dibasakan. Larutan dalam air yang
bersifat asam dan mengandung alkaloid dapat dibasakan dan alkaloid diekstraksim
dengan pelarut organik, sehingga senyawa netral dan asam yang mudah larut dalam
air tertinggal di dalam air tiroksin triftopan.
4.
Jelaskan keterkaitan diantara biosintesis, metode isolasi dan penentuan
struktur senyawa bahan alam . Berikan contohnya ?
Jawab :
Biosintesis,
metode isolasi dan penentuan struktur senyawa bahan alam sangat berkaitan.
Biosintesis
biasanya berarti suatu integrasi dari dua atau lebih elemen yang ada di dalam
suatu bahan alam dan menghasilkan suatu hasil yang baru. Hasil akhir dari suatu
proses pembentukan sebuah molekul tertentu dari prekursor kimia dan
menghasilkan suatu struktur dari suatu senyawa yang diinginkan.
Isolasi
yaitu mengambil suatu senyawa yang terdapat pada alam melalui proses dan
perlakuan tertentu. Dari proses isolasi kemudian di identifikasi hasil yang
didapatkan dari isolasi tersebut kemudian dilakukan penentuan strukturnya
melalui UV, IR, MS ataupun NMR.
sangat
terkait antara biosentesis pada kimia bahan alam dan metode isolasi dari
biosentesis kita mengetahui bagaimana suatu senyawa dihasilkan dan dengan
metode isolasi kita dapat mendapatkan senyawa yang kita inginkan dengan
mengisolasi suatu bahan yang mengandung senyawa yang kita ingin hasilkan dengan
penentuan struktur senyawa fungsinya agar kita mengetahui apakah senyawa
tersebut memiliki struktur yang sama dengan biosentesisnya.
Contohnya antara lain adalah sebagai
berikut :
Isolasi
Senyawa Terpenoid Dari Daun Tanaman Nilam (pogostemon heyneanus, benth).
1.
Ektraksi
sampel daun direndam (maserasi )
dengan menggunakan metanol + 3-4 hari. Setelah itu maserat yang diperoleh
dikumpulkan, disaring, dan dipekatkan dengan penguap bertekanan rendah hingga
diperoleh residu yang kering. Selanjutnya ekstrak yang diperoleh dipartisi
dengan menggunakan etil asetat : air = 1 :1 sebanyak 3 kali menghasilkan 2 fase
yaitu fase etil asetat dan fase air. Selanjutnya dilakukan uji reaksi liberan
buchard terhadap kedua fase. Dari uji kedua fase diketahui fase etil asetat
yang lebih memberikan hasil positif atau yang mengandung senyawa terpenid.
Kemudian dilakukan evaporasi terhadap fase vetil asetat sehingga diperoleh
ekstrak kental.
2.
Fraksinasi.
Pada
tahap ini dilajutkan dengan metode kromatografi lapis tipis (KLT) dengan
menggunakan beberapa campuran pelarut yang dilakukan terhadap ekstrak etil
asetat untuk melihat komposisi dan sistem pelarut yang tepat yang akan
digunakan dalam fraksinasi pada kromatografi kolom. Sistem pelarut antara lain
: n-heksan : etil asetat = 2 : 1, metanol : air = 5 : 1, kloroform : metanol :
air= 7 : 3 : 1. setelah diuji hasil KLT dan diperoleh sistem pelarut- ekstrak
yang tepat , selajutnya dilakukan pemisahan komponen-komponen dalam ekstrak
dengan kromatografi kolom. Sampel ekstrak yang mungkin selanjutnya dilarutkan
dengan kloroform untuk dihomogenkan dan setelah cukup kering dimasukkan kedalam
kolom danm dielusi dengan campuran n-heksan : etil asetat menurut kenaikan
gradien poleritas pelarut, mulai dari perbandingan 10 :1 sampai dengan 1 :1.
selanjutnya dilakukan kromatohgrafi lapis tipis terhadap masing-masing komponen
sehingga dihasilkan beberapa macam fraksi. Fraksi-fraksi yang mempunyai nilai
Rf yang sama digabung menjadi satu fraksi.
3.
Pemurnian
Fraksi
yang telah dikumpulkan tadi, selajunya diuapkan kemudian dilakuakan
rekristalisasi. Padatan komponen tersebut dilarutkan dengan pelarut methanol
pada suhu 50o C, kemudian disaring dengan corong buchner selagi panas. Jika
larutan berwarna, ditambahkan norit 1-2% dari berat padatan komponen tadi,
kemudian disaring kembali dan filtratnya didinginkan dalam air es sampai
terbentuk kristal.
4.
Karakterisasi
kristal
yang diperoleh uji kemurniannya dengan kromatografi lapis tipis dalam eluen
n-heksan : etil asetat (2:1) dilanjutkan dengan pengujian titik leleh dan
diidentifikasi dengan uji pereaksi Liberman – Buchard.